Materi.Co.ID – Hay hay bertemu lagi dengan artikel materi.co.id . Kali ini kita akan membahas tentang nitrogen. Simak ulasan lengkap nya dibawah ini.
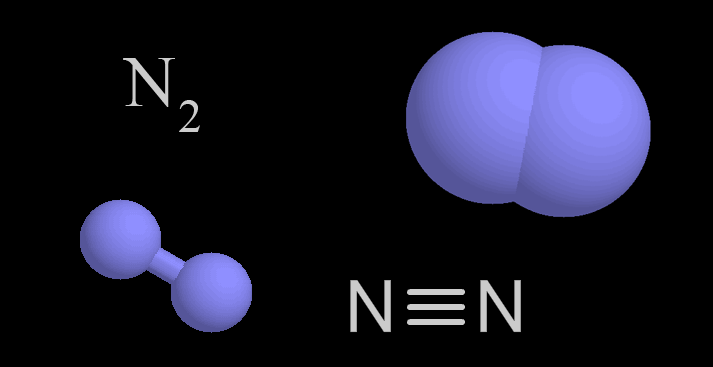
Pengertian Nitrogen
Nitrogen merupakan suatu kumpulan kelompok unsur yang tidak mengandung logan. Nitrogen sendiri membawa kandungan atom yang elektronnya berjumlah 7 buah dan kandungan protonnya juga 7 buah juga, hal ini sebagaimana pada senyawa mikroskopis nitrogen kandungan elektronnya 5 ion terletak di kulit luar sementara 2 ion elektron dan 7 lapis proton berada dalam kulit nitrogen.
Nitrogen mempunyai peran di lapisan atmosfer bumi disebabkan nitrogen mendukung kehidupan tumbuhan dan kehidupan hewan yang ada di bumi. Nitrogen mempunyai berat atom 14,0007 mikrogram yang apabila dibandingkan dengan 1 butir debu itu hanya sekitar 0,0000001 % nya saja.
Sifat – Sifat Nitrogen
1. Sifat Fisis
- Simbol: N
- Nomor atom: 7
- Berat atom: 14,007
- Klasifikasi: Gas dan bukan logam
- Fase pada Suhu Kamar: Gas
- Berat jenis: 1,251 g / L @ 0 ° C
- Titik leleh: -210,00 ° C, -346,00 ° F
- Titik didih: -195,79 ° C, -320,33 ° F
- Tidak berbau dan tidak berwarna
2. Sifat Kimia
- Nitrogen merupakan unsur yang stabil
- Di suhu rendah, nitrogen sulit bereaksi dengan unsur lain kecuali pada litium.
- Di suhu tinggi bisa bereaksi logam alkali dan alkali tanah.
- Di suhu tinggi dapat bereaksi dengan unsur nonlogam seperti oksigen dan hidrogen.
Fungsi Nitrogen
- Pengawetan makanan
Nitrogen digunakan untuk memproduksi atmosfer yang dimodifikasi di mana diaplikasikan bersama dengan karbon dioksida guna pengawetan paket atau makanan tetap segar dengan menjaga dari kerusakan oksidatif.
- Penggunaan dalam Farmasi
Gas nitrogen juga bisa digunakan untuk mengawetkan sperma, telur, saraf, darah, sel induk, dan berbagai spesimen biologis lainnya.
- Penggunaan Gas Nitrogen dalam Elektronik
Dalam indrustri manufaktur nitrogen dipakai dalam kerja internal banyak komputer dan membantu guna mencegah mereka dari pemanasan berlebih setelah berjam-jam penggunaan terus menerus.
- Penggunaan nitrogen dalam baja tahan karat
Sejumlah besar nitrogen digunakan untuk menghasilkan baja anti karat dan produk pabrik baja lainnya. Penganilan ialah perlakuan panas yang membuat baja lebih mudah diolah.
Bentuk – Bentuk Nitrogen Di Alam
- Amonia
Sumber amonia yang berada didalam perairan umumnya didapat dari pemecahan nitrogen organik (protein dan urea) dan juga nitrogen anorganik yang ada didalam air dan juga tanah, yang berasal dari dekomposisi bahan organic oleh mikroba dan juga jamur (amonifikasi).
- Nitrit
Sumber Nitrit ini bisa berupa sebuah limbah industri dan limbah domestik. Kadar Nitrit yang ada didalam wilayah perairan bersifat relatif sebab, akan segera dioksidasi menjadi sebuah Nitrat.
Nitrit merupakan sebuah bentuk peralihan yang berasal dari beberapa sumber seperti antara amonia dan nitrat (nitrifikasi), dan antara nitrat dan gas nitrogen (denitrifikasi) yang sudah terbentuk kedalam kondisi anaerob.
- Nitrat
Nitrat merupakan sumber utama dari sebuah Nitrogen yang ada di perairan, sebab sebuah Amonium lebih disukai oleh tumbuhan. Kadar Nitrat yang terdapat didalam perairan yang tidak tercemar cenderung lebih tinggi daripada dengan kadar Amoniumnya.
Selain itu, Nitrat ialah bentuk dari Nitrogen yang berfungsi sebagai sumber nutrien utama bagi pertumbuhan sebuah tanaman dan alga. Nitrat Nitrogen ini memiliki sifat yang mudah larut dan stabil didalam air.
Proses Siklus Nitrogen Biologis
Siklus nitrogen ini nantinya akan mengubah nitrogen dari satu bentuk menjadi bentuk yang lain. Sebagian besar proses perubahan ini dilakukan oleh mikroorganisme.
- Fiksasi Nitrogen
Fiksasi nitrogen ialah proses perubahan nitrogen dari atmosfer menjadi amonia. Bakteri yang berfungsi dalam proses ini ialah bakteri pada akar tanaman polongan melalui fiksasi biologis. Bakteri tersebut, antara lain seperti rhizobium dan penggunaan enzim nitrogenase cyanobacteria dikaitkan untuk mengubah gas nitrogen menjadi amonia.
Proses fiksasi juga bisa berlangsung secara kimiawi. Pengikatan nitrogen secara kimiawi juga dikenal sebagai proses pengikatan elektrokimia yang dibantu oleh energi dari halilintar.
Energi listrik yang terjadi akibat adanya halilintar akan menyebabkan gas nitrogen dan gas oksigen yang ada di atmosfer udara membentuk senyawa nitrogen dioksia (NO2).
Halilintar yang diikuti dengan hujan kemudian akan bereaksi dengan gas nitrogen dioksida sehingga membentuk asam nitrat. Sebagian ion nitrat (NO3) lalu diserap oleh akar tumbuhan, terdenitrifikasi, dan mengalami pengendapan.
- Nitrifikasi
Nitrifikasi ialah proses oksidasi biologis amonia dengan oksigen menjadi amonium lalu nitrit dan diikuti oleh proses oksidasi nitrit menjadi nitrat. Degradasi amonia yang menjadi nitrit dikenal dengan nitrifikasi.
Proses tersebut merupakan hal penting dalam siklus unsur hara tanah. Prosesnya dilakukan oleh bakteri autotrof dan bakteri amonia pengoksidasi seperti ß-Proteobacteria dan gammaproteobacteria dan bakteri amonia oksidasi dari genera nitrosomonas serta nitrosococcus.
- Asimilasi
Asimilasi nitrogen ialah proses pembentukan senyawa nitrogen organik, misalnya asam amino dari senyawa nitrogen anorganik. Sesudah proses nitrifikasi oleh bakteri, tanaman akan menyerap nitrogen dalam wujud nitrat. Lalu gradien proton transporter nitrat akan menyerap nitrat dan kemudian diteruskan oleh xilem dari akar ke tunas.
Pada tunas, reduksi nitrogen dilakukan dalam 2 langkah, yaitu nitrat akan direduksi menjadi nitrit oleh reduktase nitrat dalam sitosol. Sementara nitrit dalam kloroplas akan direduksi oleh reduktasi nitrit menjadi amonia.
- Amonifikasi
Tahapan siklus nitrogen dimana sisa-sia tanaman serta limbah terurai oleh organisme lalu menciptakan amonia disebut amonifikasi. Mikroorganisme dalam tanah akan mengurai bahan organik yang mati untuk dijadikan energi dan memproduksi amonia serta senyawa dasar lain sebagai produk sampingan. Amonia dalam tanah akan bertahan dalam bentuk ion amonium.
- Denitrifikasi
Denitrifikasi ialah proses reduksi nitrat yang berubah menjadi gas nitrogen inert dalam siklus nitrogen. Denitrifikasi dilakukan oleh bakteri seperti pseudomonas dan clostridium pada kondisi anaerobik.
Selama proses respirasi, bakteri akan menggunakan nitrat sebagai akseptor elektron. Bakteri yang mampu bertahan pada kondisi aerobik ini adalah bakteri jenis anaerob fakultatif.
Bahaya Nitrogen bagi Kesehatan Tubuh
- Membuat tubuh menjadi kekurangan vitami A
- Reaksi nitrogen dengan hemoglobin di dalam darah dapat mengakibatkan daya dukung oksigen dalam darah menurun
- Nitrogen dapat membangun nitro amina sebagai salah satu penyebab paling umum kanker
- Bisa menurunkan fungsi kelenjar tiroid
Dampak Negatif Nitrogen bagi Lingkungan
- Penambahan senyawa nitrogen dalam lingkungan mempunyai berbagai efek. Pertama, dapat mengubah komposisi spesies karena kerentanan organisme tertentu terhadap senyawa nitrogen.
- Proses pembakaran juga bisa menambahkan nitrat dan nitrit akibat emisi nitrogen oksida yang dikonversi menjadi nitrat dan nitrit oleh lingkungan.
- -Dalam lambung dan usus hewan, nitrat akan membentuk nitroamina, suatu senyawa karsinogenik berbahaya.
Isotop
Nitrogen mempunyai dua isotop yang stabi lyaitu 14N dan 15N. Isotop pertama ini lebih umum, dapat menyusun sampai 99,634% nitrogen alami, tetapi berbeda dengan yang kedua (yang sedikit lebih berat) hanya sisanya 0,366%. Hal ini mengakibatkan berat atomnya menjadi 14,007 u.
Kedua isotop stabil ini dihasilkan melalui siklus CNO didalam bintang, akan tetapi 14N lebih umum terjadi sebab tangkapan neutronnya ialah langkah pembatas laju. 14N ialah salah satu dari 5 nuklida ganjil–ganjil yang stabil (suatu nuklida yang memiliki jumlah proton dan neutron ganjil) empat lainnya ialah 10B, 2H, 6Li, dan 180mTa.
Kelimpahan relatif 14N dan 15N nyaris konstan di atmosfer, akan tetapi bisa bervariasi di tempat lain, disebabkan fraksinasi isotop alami dari reaksi redoks biologis dan penguapan amonia ataupun asam nitrat alami.
Reaksi yang dimediasi akan secara biologis (contohnya asimilasi, nitrifikasi, maupun denitrifikasi) sangat mengatur dinamika nitrogen dalam tanah. Reaksi ini biasanya menghasilkan pengayaan 15N dari substrat dan penipisan produk
Kimia dan Senyawa
Nitrogen atom, yang juga dikenal sebagai nitrogen aktif, sangat reaktif, berbentuk triradikal dan dengan 3 elektron yang tak berpasangan. Atom nitrogen bebas sangat mudah bereaksi dengan sebagian besar unsur untuk membentuk nitrida, dan bahkan ketika dua atom nitrogen bebas bertumbukan untuk memproduksi molekul molekul N2 yang tereksitasi, mereka bisa melepaskan banyak energi pada tumbukan dengan molekul stabil semacam karbondioksida dan air yang menyebabkan fisi homolitik yang menghasilkan radikal seperti CO dan O ataupun OH dan H.
Nitrogen atomik disiapkan dengan melalui aliran listrik melalui gas nitrogen pada 0,1–2 mmHg, yang memproduksi nitrogen atom bersamaan dengan emisi kuning peach dan memudar perlahan sebagai pendaran beberapa menit bahkan setelah aliranlistrik
Hidrida utama nitrogen yaitu amonia (NH3) walaupun hidrazina (N2H4) juga banyak ditemukan. Amonia mempunyai sifat basa dan terlarut sebagian dalam air membentuk ion ammonium (NH4+). Amonia cair ini sebenarnya sedikit amfiprotik kemudian membentuk ion ammonium, dan amida (NH2-) atau yang disebut juga garam amida, dan nitrida (N3-), namun terurai dalam air.
Gugus bebas amonia dengan atom hidrogen tunggal ataupun ganda dsebut dengan nama amina. Rantai, cincin atau struktur hidrida nitrogen yang lebih besar diketahui namun tidaklah stabil.
Demikianlah bahasan kita mengenai nitrogen. Terima kasih bagi yang menyempatkan waktu untuk membaca dan mampir di artikel √ Sifat – Sifat Nitrogen : Pengertian, Bentuk & Dampaknya Lengkap. Semoga bermanfaat dan menambah wawasan kamu ?
Baca Juga Artikel Lainnya
- √ Sifat – Sifat Oksigen : Pengertian, Fungsi, Struktur & Sifatnya Lengkap
- √ Dampak Karbon Dioksida : Pengertian, Sifat & Dampaknya Lengkap
- √ Jenis – Jenis Kapasitor : Pengertian, Fungsi & Rumusnya Lengkap
- √ Fungsi Resistor : Pengertian, Jenis & Kodenya Terlengkap
- √ Faktor – Faktor Viskositas : Pengertian, Rumus & Tipenya Lengkap