Materi.Co.ID – Hay hay bertemu lagi dengan artikel materi.co.id . Kali ini kita akan membahas tentang ikatan ion. Simak ulasan lengkap nya dibawah ini.
Pengertian Ikatan Ion
Ikatan ion merupakan ikatan yang terbentuk dikarenakan adanya gaya tarik menarik secara elektrostatis yang berlangsung di antara ion positif dan negatif.
Atom yang energi ionisasinya rendah akan lebih mudah membentuk ion positif sebab melepaskan elektron. Selanjutnya elektron tersebut ditangkap oleh atom yang mempunyai afinitas elektron yang besar membentuk ion negatif sebab ia mudah menerima elektron. Maka akan terjadi gaya tarik menarik dan terbentuklah senyawa yang bersifat netral.
Sifat – Sifat Ikatan Ion
Selain bersifat relatif kuat, ikatan ion juga mempunyai sifat-sifat yang lain, diantaranya ialah sebagai berikut :
- Mempunyai titik didih dan titik leleh yang tinggi. Ion positif dan negatif dalam kristal senyawa ion tidak bebas bergerak sebab terikat oleh gaya elektrostatik yang kuat. Diperlukan suhu yang tinggi agar ion-ion mendapatkan energi kinetik yang cukup untuk mengatasi gaya elektrostatik.
- Keras tetapi rapuh. Memiliki sifat keras sebab ion-ion positif dan negatif terikat kuat ke segala arah oleh gaya elektrostatik. Bersifat rapuh disebabkan lapisan-lapisan dapat bergeser apabila dikenakan gaya luar, ion sejenis dapat berada satu di atas yang lainnya maka timbul tolak-menolak yang sangat kuat yang mengakibatkan terjadinya pemisahan.
- Berupa padatan pada suhu ruang.
- Larut dalam pelarut air, namun umumnya tidak larut dalam pelarut organik
- Tidak menghantarkan listrik dalam fasa padat, namun bisa menghantarkan listrik dalam fasa cair. Zat dikatakan bisa menghantarkan listrik jika terdapat ion-ion yang bisa bergerak bebas membawa muatan listrik.
Ciri – Ciri Ikatan Ion
Terdiri dari atom logan dan non-logam.
Atom Logam :
- Besi (Fe)
- Alumunium (Al)
- Perak (Ag)
- Emas (Au)
- Natrium (Na)
- Magnesium (Mg)
- Lithium (Li)
- Logam dari gol IA(1A) dan IIA(2A)
Atom Non-Logam :
- Karbon (C)
- Hidrogen (H)
- Oksigen (O)
- Nitrogen (N)
- Phosfor (P)
- Dll
- Unsur dari gol VA, VIA, VIIA
Pembentukan Ikatan Ion
Setiap unsur harus berusaha memiliki konfigurasi elektron seperti gas mulia, dapat dengan melepaskan elektron ataupun menerima elektron.
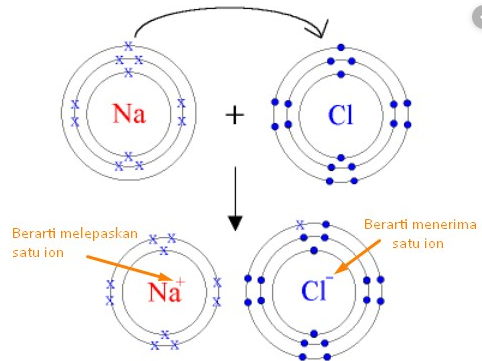
Peristiwa serah terima elektron ini berlangsung pada senyawa NaCl alias garam dapur. Na merupakan golongan IA dimana ia mempunyai elektron valensi 1, maka agar stabil ia harus melepas 1 elektron. Apabila dilihat dari konfigurasi elektronnya, 11Na: 2, 8, 1. Maka apabila melepas 1 elektron, maka elektron paling terakhinya menjadi 8 (sesuai kaidah oktet). Sebab melepas 1 elektron, maka Na yang asalnya netral berubah menjadi bermuatan +1 (Na+). Reaksinya :
Na → Na+ + e– (artinya Na melepas 1 elektron)
1 elektron tadi yang dilepas Na? hilang kah? Tidak, disana ada yang menangkapnya yakni si Cl. Dikarenakan Cl mempunyai elektron valensi 7 (dia golongan VIIA). Apabila dilihat dari konfigurasi elektronnya 17Cl : 2, 8, 7. Jadi apabila Cl menangkap 1 elektron, konfigurasinya akan menjadi 2, 8, 8, dengan elektron terakhirnya 8, ini sudah mematuhi kaidah oktet. Sebab Cl menangkap 1 elektron maka Cl yang asalnya netral berubah menjadi -1 (Cl–). Reaksinya:
Cl + e– → Cl– (berarti Cl menerima 1 elektron, lihat elektron berada di sebelah kiri panah)
Adakah pengaruhnya pembentukan Na+ dan Cl– ini? Sesuai hukum Coulomb, muatan yang berbeda jenis akan saling tarik menarik. Jadi Na+ ini akan berikatan dengan Cl– dengan gaya elektrostatik.
Na+ + Cl– → NaCl
Ikatan ion = logam + nonlogam
Apabila digeneralisir, ikatan logam itu diantaranya yakni Golongan IA (kecuali H), IIA (kecuali Be), IIIA (Aluminium), golongan transisi (Golongan B). Sedangkan nonlogam, diantaranya golongan IVA-VIIA, kalo VIIIA relatif stabil.
Demikianlah bahasan kita mengenai ikatan ion. Terima kasih bagi yang menyempatkan waktu untuk membaca dan mampir di artikel √ Ciri – Ciri Ikatan Ion : Pengertian, Sifat & Pembentukannya Lengkap. Semoga bermanfaat dan menambah wawasan kamu ?
Baca Juga Artikel Lainnya
- √ Sifat Koligatif Larutan : Pengertian, Sifat, Rumus & Contohnya Lengkap
- √ Prinsip Kromatografi : Pengertian & Jenisnya Lengkap
- √ Bahaya Kloroform : Pengertian, Reaksi & Penggunaannya Lengkap
- √ Jenis – Jenis Larutan : Pengertian, Jenis, Kadar & Reaksinya Lengkap
- √ Kegunaan Logam Alkali : Pengertian & Sifatnya Lengkap