Materi.Co.ID – Hay hay bertemu lagi dengan artikel materi.co.id . Kali ini kita akan membahas tentang asam asetat. Simak ulasan lengkap nya dibawah ini.
Pengertian Asam Asetat
Asam asetat atau asam etanoat merupakan senyawa kimia organik terbaik dkarenakan memberikan rasa asam pada cuka dan bau yang tajam.
Asam asetat ialah salah satu asam karboksilat paling sederhana (kedua-paling sederhana, setelah asam format) dan mempunysi rumus kimia CH3COOH. Pada keadaan murni, keondisi bebas air-nya, yang dinamai asam asetat glasial, itu ialah, cairan higroskopis tak berwarna yang membeku di bawah 16,7 ° C (62 ° F) ke kristal padat tak berwarna.
Asam asetat memiliki sifat korosif, dan uap yang mengiritasi mata, menciptakan rasa panas di hidung, dan bisa mengakibatkan sakit tenggorokan dan paru-paru tersumbat. Istilah asetat dipakai sewaktu mengacu pada anion karboksilat (CH3COO-) atau salah satu dari garam atau ester asam asetat.
Fungsi Asam Asetat
- Sebagai pereaksi kimia, Pereaksi kimia dilakukan untuk menciptakan berbagai jenis senyawa kimia. Asam asetat juga umumnya digunakan untuk produksi monumel vinil. Selain itu digunakan juga untuk pereaksin kimia yang lainnya
- Produksi polimer, Petan asam asetat dalam produksi polimer ini sangat membantu, karena itu harus digunakannya asam asetat ini.
- Sebagai pengatur keasaman, umumnya asam asetat digunakan sebagai pengatur keasaman pada industri makanan
- Sebagai pelunak air, apabila dalam industri makanan kebanyakan asam asetat digunakan untuk mengatur keasaman, beda dengan dirumah tangga umumnya asam asetat digunakan sebagai pelunak air
- Minuman fungsional, asam asetat digunakan untuk minuman fungsional, misalnya cuka apel. dan minuman fungsional lainya
- Bahan baku membuat bahan kimia, sering juga digunakan untuk membuat bahan baku kimia, akan tetapi harus disesuaikan dengan keperluannya
- Digunakan kedalam produksi ester
- Produksi anhidrida asetat
Sifat – Sifat Kimia Asam Asetat
- Keasaman
Atom hidrogen (H) pada gugus karboksil (−COOH) dalam asam karboksilat seperti asam asetat bisa dibebaskan sebagai ion H+ (proton), maka memberikan sifat asam. Asam asetat ialah asam lemah monoprotik dengan nilai pKa=4.8. Basa konjugasinya ialah asetat (CH3COO−). Sebuah larutan 1.0 M asam asetat (kira-kira sama dengan konsentrasi pada cuka rumah) mempunyai pH sekitar 2.4.
- Dimer Siklis
Struktur kristal asam asetat menjelaskan bahwa molekul-molekul asam asetat berpasangan membentuk dimer yang dikaitkan oleh ikatan hidrogen. Dimer juga bisa dideteksi pada uap bersuhu 120 °C. Dimer juga berlangsung pada larutan encer di dalam pelarut tak-berikatan-hidrogen, dan seringkali pada cairan asam asetat murni. Dimer akan dirusak dengan adanya pelarut berikatan hidrogen (contohnya air). Entalpi disosiasi dimer tersebut diperkirakan antara 65.0–66.0 kJ/mol, entropi disosiasi sekitar 154–157 J mol−1 K−1. Sifat dimerisasi ini juga dimiliki oleh asam karboksilat sederhana lainnya.
- Sebagai Pelarut
Asam asetat cair ialah pelarut protik hidrofilik (polar), mirip seperti air dan etanol. Asam asetat mempunyai konstanta dielektrik yang sedang yakni 6.2, sehingga ia bisa melarutkan baik senyawa polar seperi garam anorganik dan gula maupun senyawa non-polar seperti minyak dan unsur-unsur seperti sulfur dan iodin. Asam asetat akan bercampur dengan mudah dengan pelarut polar atau nonpolar lainnya seperti air, kloroform dan heksana. Sifat kelarutan dan kemudahan bercampur dari asam asetat ini membuatnya dipergunakan secara luas dalam industri kimia.
- Reaksi-reaksi Kimia
Asam asetat bersifat korosif terhadap banyak logam seperti besi, magnesium, dan seng, membentuk gas hidrogen dan garam-garam asetat (dinamai logam asetat). Logam asetat juga bisa diidapatkan dengan reaksi asam asetat dengan suatu basa yang cocok. Misalnya ialah reaksi soda kue (Natrium bikarbonat) bereaksi dengan cuka. Hampir semua garam asetat larut dengan baik dalam air. Salah satu pengecualian ialah kromium (II) asetat. Contoh reaksi pembentukan garam asetat:
» Mg(s) + 2 CH3COOH(aq) → (CH3COO)2Mg(aq) + H2(g)
» NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l)
Aluminium merupakan logam yang tahan pada korosi sebab bisa membentuk lapisan aluminium oksida yang melindungi permukaannya. Karena itu, umumnya asam asetat diangkut dengan tangki-tangki aluminium.
Asam asetat mengalami reaksi-reaksi asam karboksilat, contohnya menciptakan garam asetat apabila bereaksi dengan alkali, menciptakan logam etanoat bila bereaksi dengan logam, dan menciptakan logam etanoat, air dan karbondioksida jika bereaksi dengan garam karbonat atau bikarbonat.
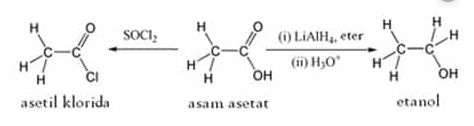
Reaksi organik yang paling terkenal dari asam asetat ialah pembentukan etanol melalui reduksi, pembentukan turunan asam karboksilat seperti asetil klorida atau anhidrida asetat melalui substitusi nukleofilik. Anhidrida asetat dibentuk melewati kondensasi 2 molekul asam asetat. Ester dari asam asetat dapat didapat melalui reaksi esterifikasi Fischer, dan juga pembentukan amida. Disuhu 440 °C, asam asetat akan terurai menjadi metana dan karbon dioksida, atau ketena dan air.
- Deteksi
Asam asetat bisa dikenali dengan baunya yang khas. Selain itu, garam-garam dari asam asetat dapat bereaksi dengan larutan besi(III) klorida, yang menciptakan warna merah pekat yang hilang apabila larutan diasamkan. Garam-garam asetat jika dipanaskan dengan arsenik trioksida (AsO3) membentuk kakodil oksida ((CH3)2As-O-As(CH3)2), yang mudah dikenali dengan baunya yang tidak sedap.
Bahaya Asam Asetat
- Jangan menelan. Hindari kulit serta kontak mata. Hindari pajanan terhadap uap atau kabut.
Potensi Efek Kesehatan: - Mata: Bisa mengakibatkan iritasi.
- Kulit: Bisa mengakibatkan iritasi.
- Tertelan: Bisa mengakibatkan ketidaknyamanan pencernaan.
- Penghirupan: Bisa mengakibatkan iritasi pada saluran pernapasan.
Pembentukan Asam Asetat
Asam Asetat diciptakan dari cairan piroligneous yang didapat dari distilasi kayu. cairan ini direaksikan dengan kalsium hidroksida menciptakan kalsium asetatselanjutnya diasamkan dengan asam sulfat lalu menghasikan asam asetat. Dari keterangan diatas menjelaskan bahwa Reaksi yang terjadi dalam proses pembuatan asam asetat termasuk Reaksi Netralisasi Asam Basa.
![]()
1. Sistem Periodik dasar Pada Unsur
Dasar Element Asam Asetat dengan sistem periodik yang sekarang digunakan ialah sistem periodik panjang. Asam asetet memiliki rumus molekul CH3COOH. dengan kata lain unsur dasar elementnya ialah unsur C, H, O dengan urutan C, H3, C, O, O, dan H. Dan ini merupakan penjelasan tentang unsur dasar element dari asam asetat.
- C = Karbon
- H = Hidrogen
- O = Oksigen
Analisis : jadi unsur dasar element yang berhubungan pada asam asetat ialah unsur Karbon, Hidrogen, dan Oksigen.
2. Sifat Periodik Unsur
dalam hal ini sifat periodik yang beradadalam asam asetat ialah Sifat logam. yang di bagi menjadi 3 yaitu. logam, nonlogam dan semilogam. pada asam asetat termasuk sifat Nonlogam. Disebabkan tidak menghantarkan listrik. dam bersifat Senyawa organik dan pada tabel unsur periodik di jelaskan bahwa senyawa pada unsur dasar asam asetat ialah nonmetals/nonlogam.
Demikianlah bahasan kita mengenai asam asetat. Terima kasih bagi yang menyempatkan waktu untuk membaca dan mampir di artikel √ Asam Asetat : Pengertian, Fungsi, Sifat, Bahaya & Pembentukannya Lengkap. Semoga bermanfaat dan menambah wawasan kamu ?
Baca Juga Artikel Lainnya
- √ Asam Nukleat : Pengertian, Fungsi, Struktur, Sifat & Jenisnya Lengkap
- √ Asam Absisat : Pengertian, Fungsi & Cara Kerjanya Lengkap
- √ Asam Amino : Pengertian, Jenis, Struktur & Sifatnya Lengkap
- √ Asam Basa : Pengertian, Teori, Reaksi & Indikatornya Lengkap
- √ Asam Sulfat : Pengertian, Sifat, Reaksi & Kegunaannya Lengkap